Release-Highlights für Prüfzentren
Erscheinungsdatum: 17. April 2026
Die Version 26R1.0 der Veeva -Produkte für Prüfzentren ist ab dem 17. April 2026 verfügbar. Die wichtigsten Neuerungen sind unten zusammengefasst. Die vollständigen Versionshinweise finden Sie gegebenenfalls über den Link im jeweiligen Produktbereich.
Veeva eCOA
Klicken Sie hier, um eine vollständige Liste der Neuerungen in Veeva eCOA in dieser Version anzuzeigen.
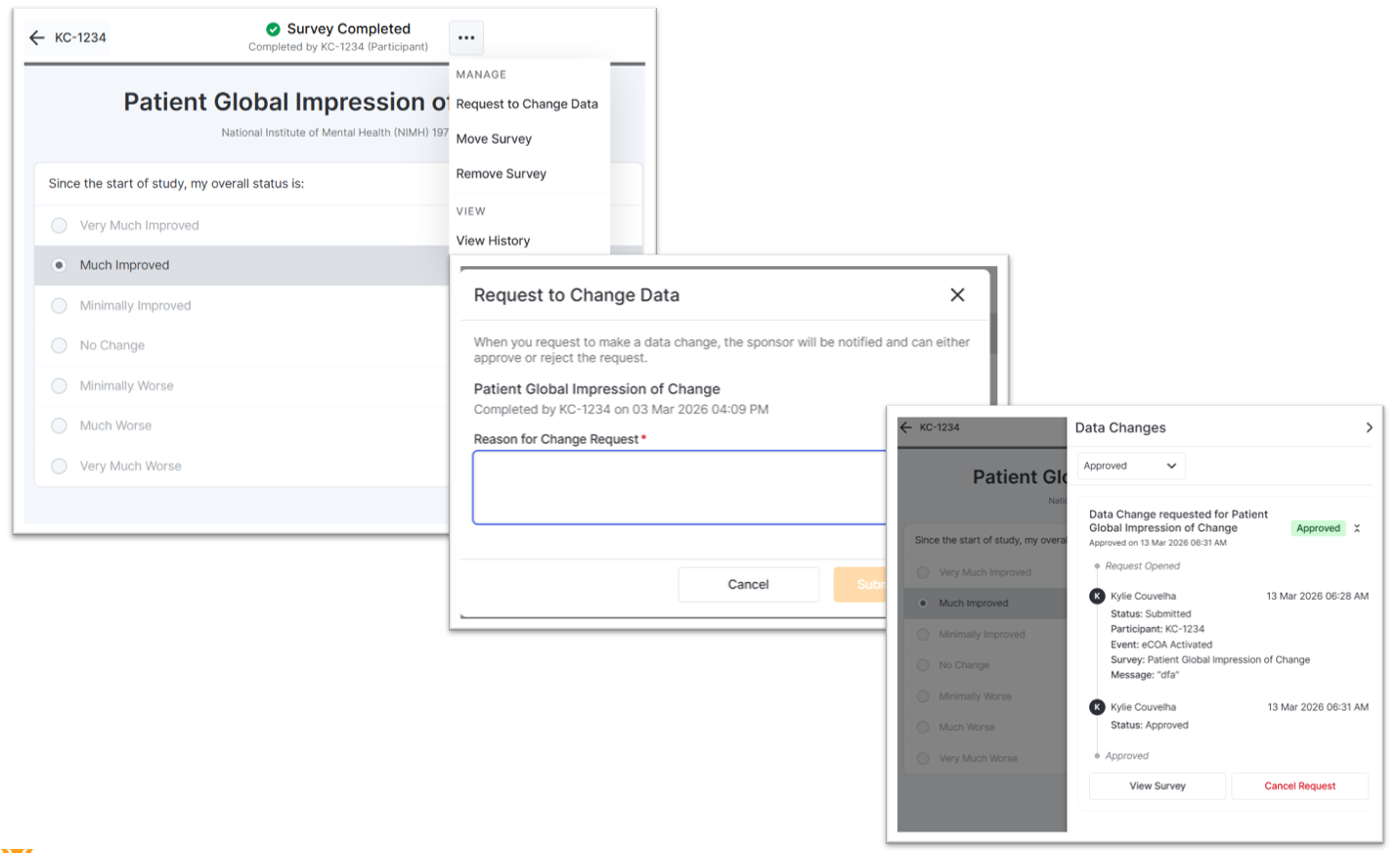
Gezielte Datenänderungen
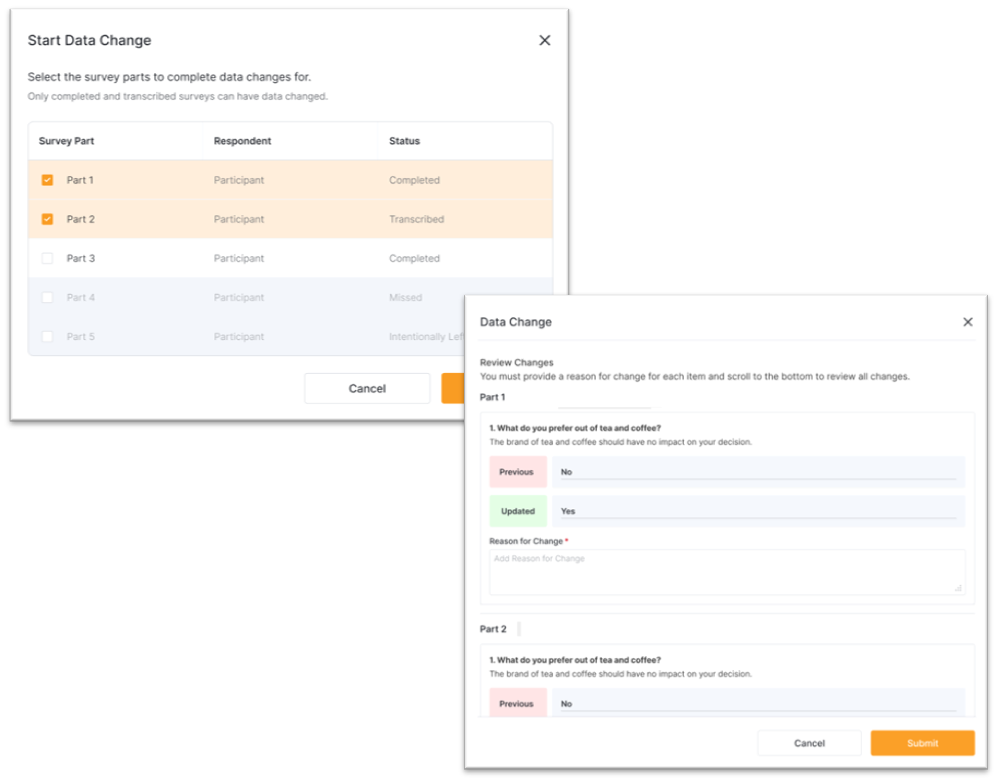
Sie können Änderungsanträge für jede Umfrage einreichen, sobald Datenänderungen deaktiviert sind oder die Frist für Änderungen abgelaufen ist. Der Auftraggeber/CRO prüft, genehmigt oder lehnt diese Anträge ab. Nach Genehmigung eines Änderungsantrags können Sie die Änderung in der entsprechenden Umfrage vornehmen.
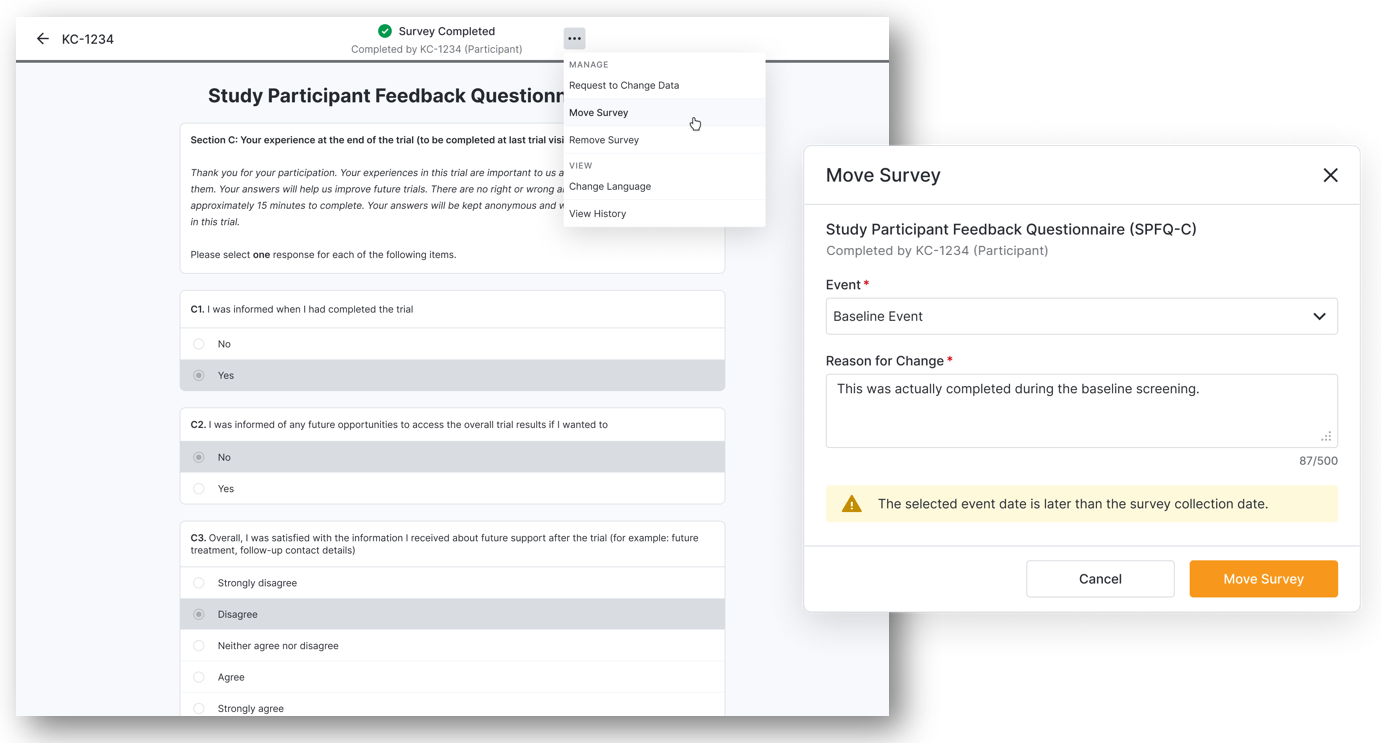
Verschieben abgeschlossener Umfragen
Sie können nun eine abgeschlossene Umfrage einer anderen Veranstaltung zuordnen, wenn sie für die falsche Veranstaltung ausgefüllt wurde. Nach der Zuordnung können wir überschneidende, verfügbare oder verpasste Umfragen für die Zielveranstaltung stornieren und sicherstellen, dass alle Änderungen im Prüfprotokoll erfasst werden. Sie müssen keine Datenänderungsanträge mehr einreichen, um Umfragen einer anderen Veranstaltung zuzuordnen.
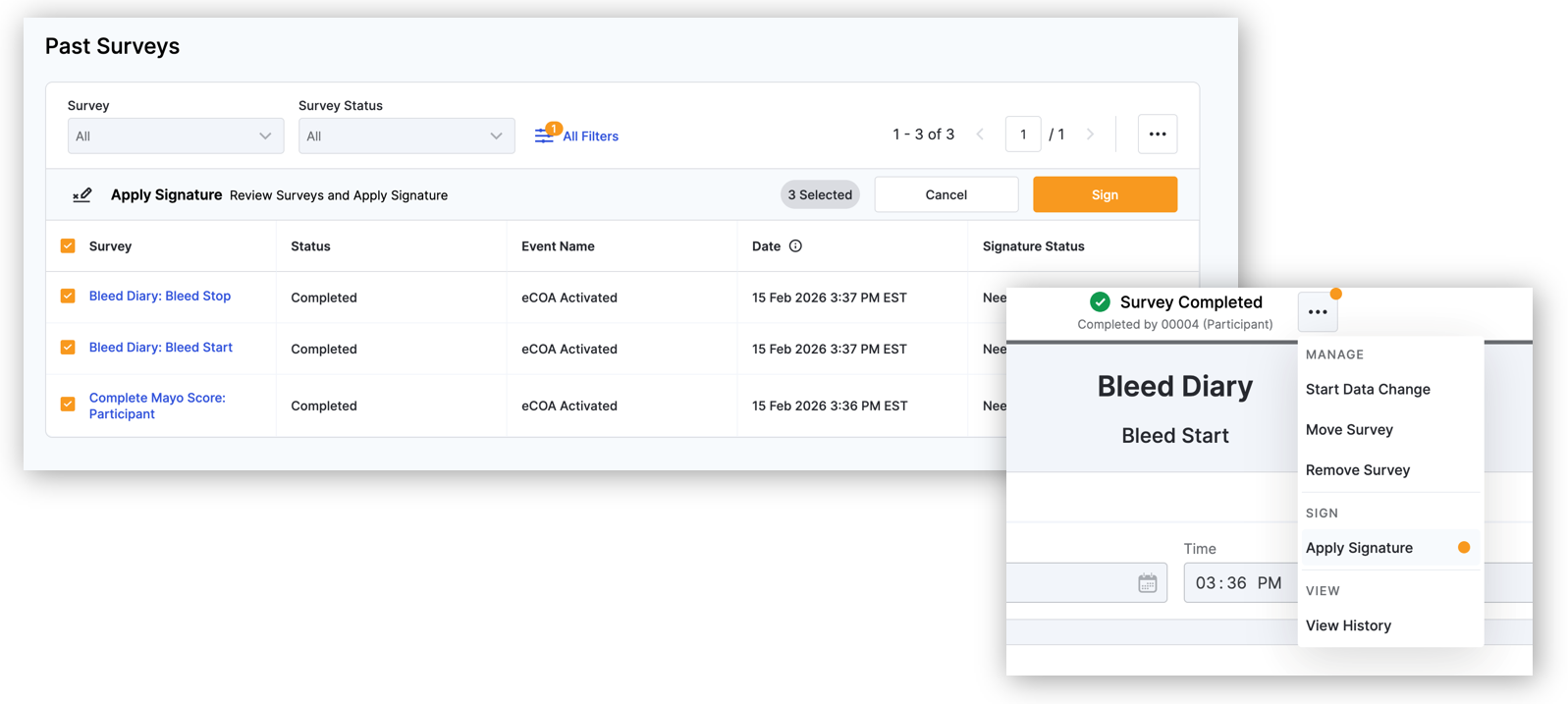
Datenprüfung und Unterschrift des Prüfzentrum
Wenn ein Sponsor/CRO von einem Prüfarzt verlangt, die Daten auf Vollständigkeit und Richtigkeit zu überprüfen, können die Prüfärzte elektronisch mit ihren VeevaID Zugangsdaten bestätigen, dass sie die Daten geprüft haben.
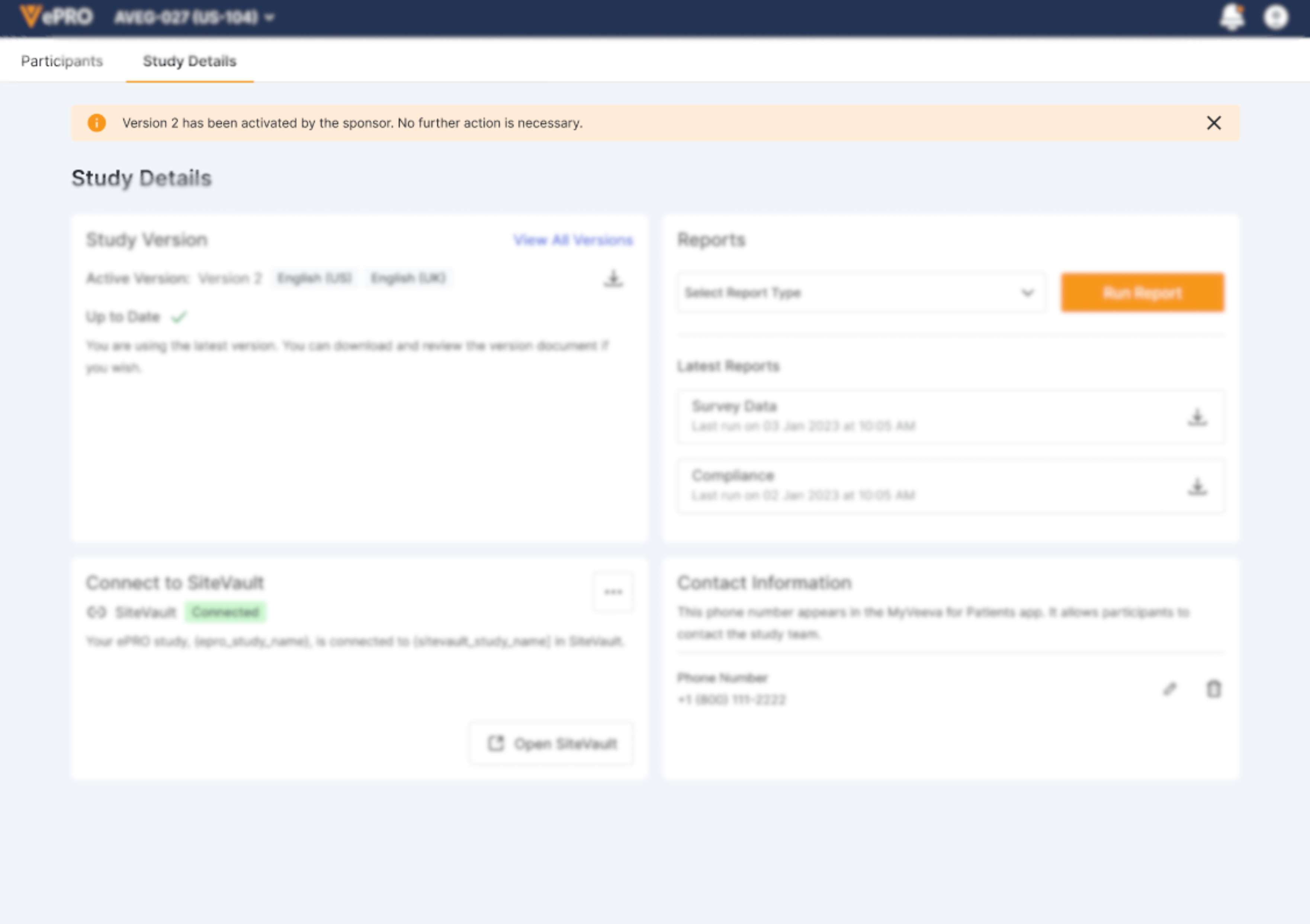
Sponsorgesteuerte Bereitstellung
Sponsoren/CROs können eine genehmigte Studienversion bereitstellen und aktivieren. Falls Sie eine Studie aktivieren müssen, wird Ihnen weiterhin ein Banner am oberen Bildschirmrand angezeigt.
Mehrteilige Umfragen
Umfragen können vom Sponsor/CRO so konfiguriert werden, dass sie aus mehreren Teilen bestehen. Beim Ausfüllen einer mehrteiligen Umfrage können Sie frühere Teile einreichen und einsehen. Wenn Sie Umfragedaten ändern, können Sie auswählen, an welchen Teilen die Änderung vorgenommen werden soll.
Zusammengesetzte Erhebungen
Zusammengesetzte Umfragen werden vom Auftraggeber/CRO so konfiguriert, dass für jeden Teil ein anderer Befragter zuständig ist. Beim Betrachten einer solchen Umfrage sehen Sie Teile, die von verschiedenen Befragten, z. B. Studienteilnehmern und anderem Prüfzentrum, ausgefüllt wurden. Wenn Sie Umfragedaten ändern, können Sie auswählen, auf welche Teile die Änderung angewendet werden soll.
Veeva EDC
Hier auswählen Eine vollständige Liste der Neuerungen in dieser Version von Veeva EDC finden Sie hier.
Alle Formulardaten löschen
Beim Zurücksetzen von Ereignissen und Formularen mit externen Daten ist nun ein zweistufiges Verfahren erforderlich. Dieses zweistufige Verfahren bietet mehr Kontrolle und Schutz beim Entfernen von Daten und reduziert die Notwendigkeit, dass externe Systeme die Daten erneut senden müssen.
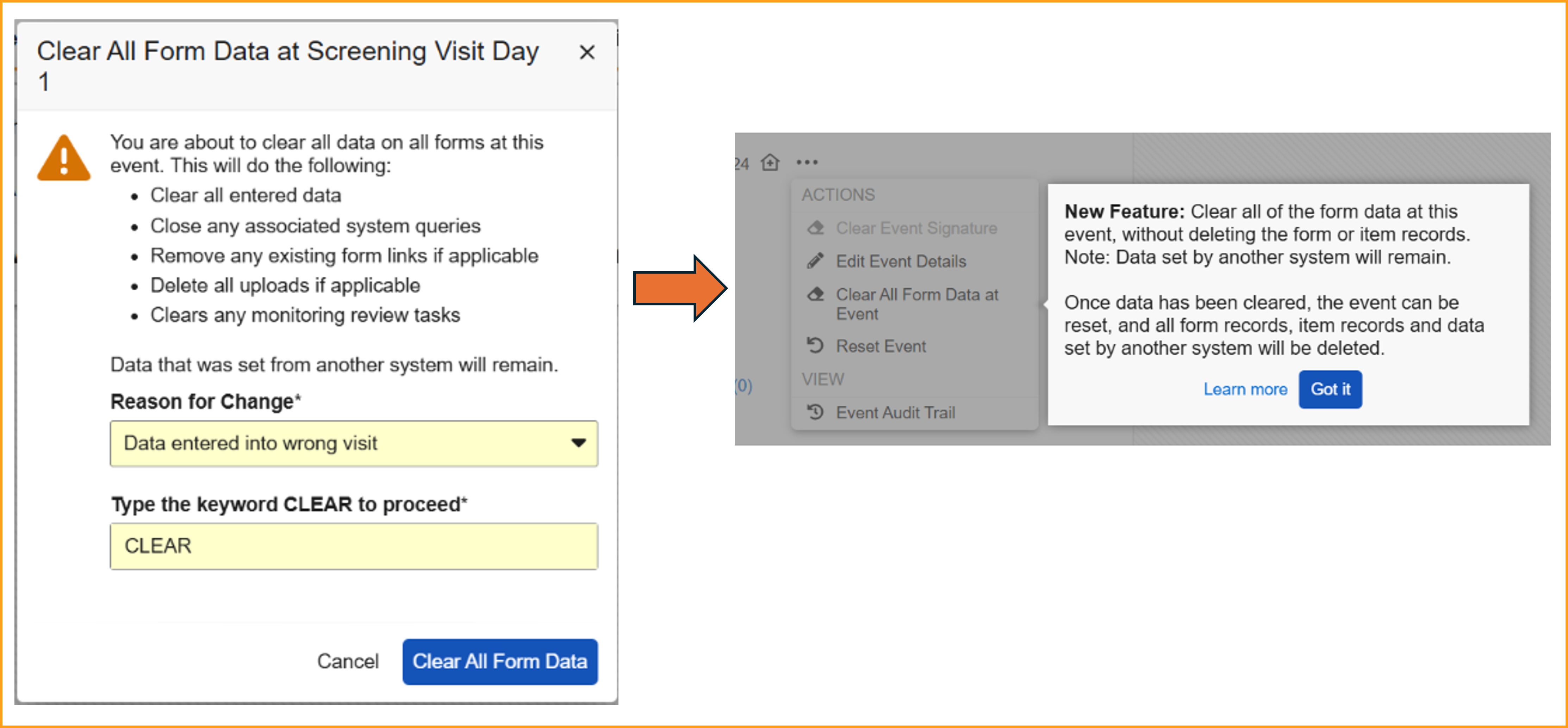
Bei Veranstaltungen mit einem oder mehreren Formularen, die Daten enthalten, wird im Menü „Veranstaltungsaktionen“ die neue Option „ Alle Formulardaten bei Veranstaltung löschen“ angezeigt. Dadurch können Prüfzentren die Formulardaten zurücksetzen und gleichzeitig die von externen Systemen gesendeten Daten, wie z. B. IRT-Daten, schützen.
Beim Löschen von Formulardaten bleiben die Ereignisdaten, die Besuchstermin und alle externen Daten erhalten. Falls auch diese Daten entfernt werden müssen, verwenden Sie die Option „Ereignis zurücksetzen“. Das Dialogfenster für diese Option wurde aktualisiert und bietet nun detailliertere Informationen zum Ablauf.
Beim ersten Aufruf des Menüs „Aktionen“ nach der Veröffentlichung wird den Nutzern der Prüfzentrum ein Dialogfenster mit Hilfetexten angezeigt, in dem die neue Funktion erläutert wird.
Veeva Site Connect
Hier klicken, um eine vollständige Liste der Neuerungen in Veeva Site Connect dieser Version anzuzeigen.
FDA 1572 generieren
Diese Funktion ermöglicht die Generierung eines FDA-Formulars 1572 innerhalb von Site Connect. Durch die Nutzung vorhandener CTMS Daten – insbesondere Informationen aus dem Prüfzentrum wie Prüfzentrum und Prüfzentrum – füllt das System das Formular automatisch aus.
Site Connect Nutzer können das Formular über einen neuen Formular-Tab auf der Dokumentenaustauschseite verwalten. Die Benutzeroberfläche ist in Abschnitte unterteilt, die dem Layout des physischen FDA-Formulars 1572 entsprechen, und bietet dynamische Bearbeitungsmöglichkeiten. Nutzer können fehlende Informationen manuell ergänzen, z. B. neue Prüfzentrum hinzufügen oder nicht zutreffende, vorausgefüllte Adressen entfernen. Das Dokument kann auch direkt in der Site Connect Benutzeroberfläche elektronisch signiert werden. Alternativ können Prüfzentrum das Formular herunterladen, bearbeiten und manuell signieren, falls eine handschriftliche Unterschrift erforderlich ist, und das ausgefüllte Dokument anschließend wieder hochladen.
Wenn die Prüfzentrum mit SiteVault verbunden ist, kann das Formular 1572 automatisch im ISF eingereicht werden.
Die Site Connect -Dokumentansicht für veraltete und gelöschte Statustypen wurde entfernt.
Diese Funktion verhindert, dass Prüfzentrum -Benutzer auf den Inhalt ausgetauschter Dokumente zugreifen können, die einen Lebenszyklusstatus erreicht haben, der mit den Statustypen „Veraltet“ oder „Gelöscht“ verknüpft ist.
Die Dokumentenzeile bleibt im Bereich „Dokumentenaustausch“ sichtbar, der Inhalt selbst ist jedoch eingeschränkt. Wählt ein Benutzer den Namenslink aus, zeigt der Dokumentenbetrachter an, dass das Dokument nicht mehr verfügbar ist.
Das gleiche Verhalten gilt auch für die Auswahl von Dokumentlinks in E-Mail-Benachrichtigungen zum Dokumentenaustausch.
Verbesserungen der Benutzeroberfläche der Prüfzentrum
Diese Funktion fügt der Startseite der Prüfzentrum mehrere Verbesserungen der Benutzeroberfläche hinzu.
- Die Spaltenreihenfolge in „Studie “ wurde aktualisiert, um eine intuitivere Darstellung der Kontaktinformationen zu ermöglichen. Die E-Mail-Adresse erscheint nun direkt nach „Ansprechpartner für“, und die Telefonnummer im Büro wurde in „Büro“ umbenannt.
- Beim Überfahren eines zurückgerufenen Dokuments im Dokumentenaustausch mit der Maus wird nun dynamisch der vom Sponsor oder CRO angegebene Rückrufgrund angezeigt. Zuvor wurde eine allgemeine Meldung angezeigt, die besagte, dass das Dokument nicht mehr zugänglich sei.
- Die Fehlermeldungen wurden standardisiert, wenn ein Download entweder über den PAL-Dokumentenbetrachter oder über Authenticated Document Links fehlschlägt.
Fehlgeschlagene Sicherheitsverteilungen auf der Prüfzentrum sichtbar
Sicherheitsverteilungen im Status „Fehlgeschlagen“ sind nun in der Sicherheitsverteilung und im Dokumentenaustausch sichtbar. Empfänger, die Verteilungsaufgaben abschließen, können die Dokumente als „ Gelesen“ markieren. Dies ermöglicht eine bessere Übersicht und Verwaltung der ausgetauschten Sicherheitsdokumente.
Veeva SiteVault
Klicken Sie hier, um eine vollständige Liste der Neuerungen in dieser Version von Veeva SiteVault anzuzeigen.
Neu gestaltetes digitales Delegationsprotokoll
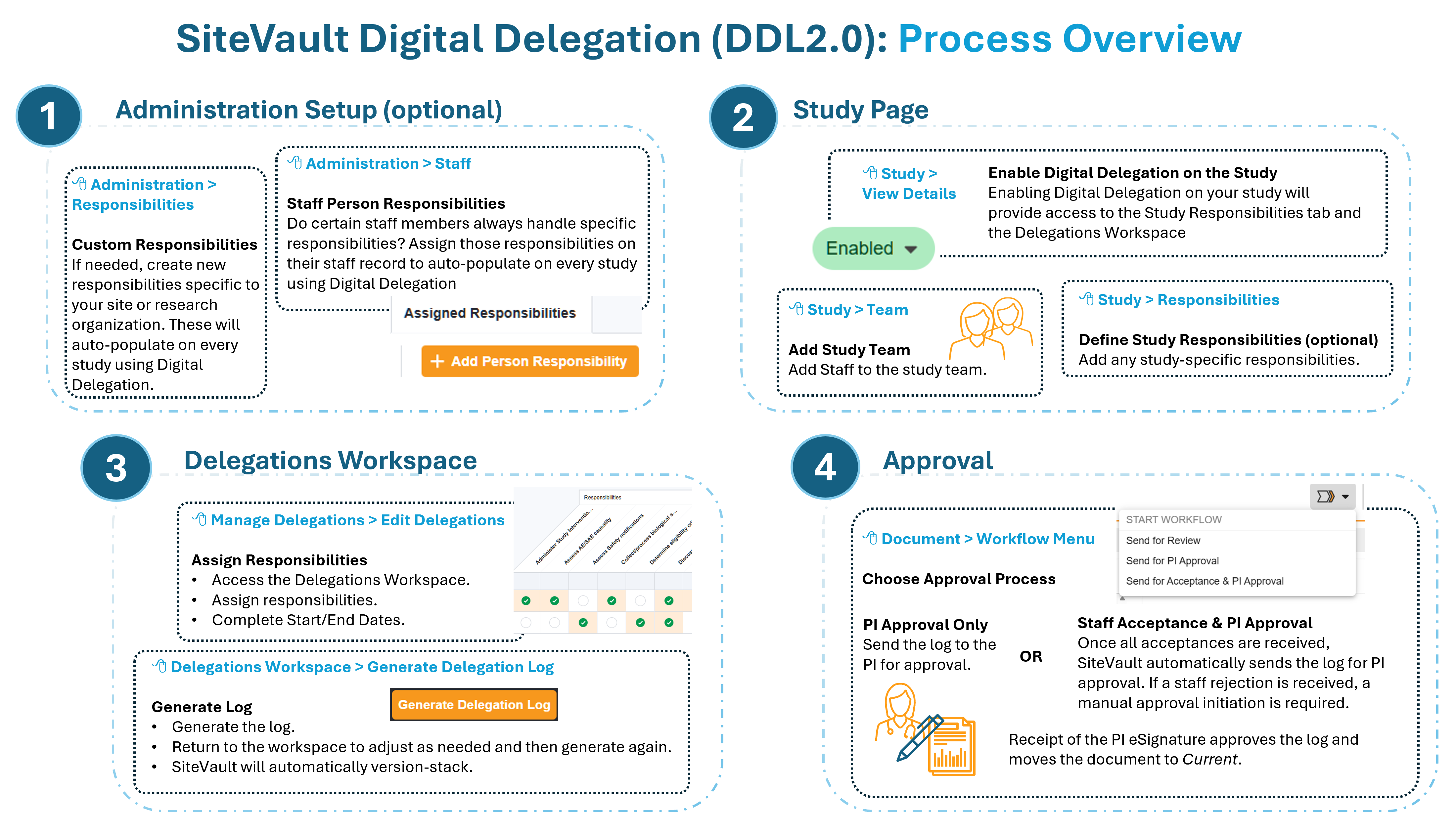
Wir freuen uns, Ihnen eine überarbeitete Version der digitalen Delegierung vorzustellen, die ein umfangreiches Update bietet und Ihnen mehr Flexibilität und Effizienz bei der Verwaltung von Delegierungsprotokollen in SiteVault ermöglicht.
- Delegationen verwalten: Der Reiter „Team“ der Studie enthält nun eine Schaltfläche „Delegationen verwalten“, die zum Delegationseditor führt. Dieser intuitive Arbeitsbereich ermöglicht die Verwaltung von Mitarbeiterverantwortlichkeiten und Start-/Enddaten in Echtzeit und bietet jederzeit einen klaren Überblick über die Delegationen Ihrer Studie.
- Flexible Genehmigungen: Prüfzentren haben nun die Möglichkeit, DOA-Protokolle direkt an den PI zur Unterschrift zu senden oder einen Genehmigungsschritt durch Mitarbeiter einzubauen, je nach dem Prüfprozess Ihres Standorts.
- Inaktive Teammitglieder: Sie können nun die Delegationsdaten für inaktive Studienteammitglieder direkt verwalten und korrigieren, um sicherzustellen, dass Ihre Protokolle während des gesamten Studienlebenszyklus korrekt bleiben.
- Verbesserte DOA-Erfahrung: Die aktualisierte eDOA-Ausgabe verfügt über ein anklickbares Inhaltsverzeichnis für eine schnellere Navigation und eine standardisierte E-Signaturseite für eine verbesserte Compliance-Dokumentation.
Aktuelle DDL-Nutzer finden weitere Informationen im Digital Delegation 2.0 Transition Guide.
Unterschrift Prüfzentrum
Um den Genehmigungsprozess zu vereinfachen, wenn eine Unterschrift Prüfzentrum nicht erforderlich oder angebracht ist, können Mitarbeiter ausgefüllte eConsent Einwilligungsformulare ohne Gegenzeichnung genehmigen. Bei der Aufgabe „ Prüfzentrum signieren oder ablehnen“ wird die eConsent durch Auswahl der Option „Aktualisieren ohne Unterschrift“ sofort genehmigt, wodurch die Abfrage der Prüfzentrum und die Erstellung einer elektronischen Unterschrift entfällt. Damit eine eConsent keine Unterschrift Prüfzentrum erfordert, darf die Rolle „Unterzeichner des Prüfzentrum “ während der Bearbeitung der eConsent nicht ausgewählt sein.
Studie: Ausgabenplan
Der Kostenplan (Menü „Finanzen“) ermöglicht die Erfassung der Studienkosten pro Besuch und Teilnehmer. So können Sie fundierte Entscheidungen bei der Budgetverhandlung mit den Sponsoren treffen. Kostenpläne werden, wie CTMS Zeitpläne und -Budgets, versionskontrolliert. Sobald Kosten im Kostenplan nach Abschluss der Besuchstermine anfallen, werden automatisch zahlbare Positionen generiert und auf der neuen Registerkarte „Zahlbare Positionen“ erfasst.
Die Funktion bietet Unterstützung für drei primäre Ausgabenkategorien:
- Aktivitätskosten: Kosten für die Durchführung der Studienverfahren.
- Personalkosten: Stundenaufwand und Kosten des wichtigsten Studienpersonals.
- Teilnehmervergütungen Kosten der Teilnehmervergütung.
Kalender Besuchstermin
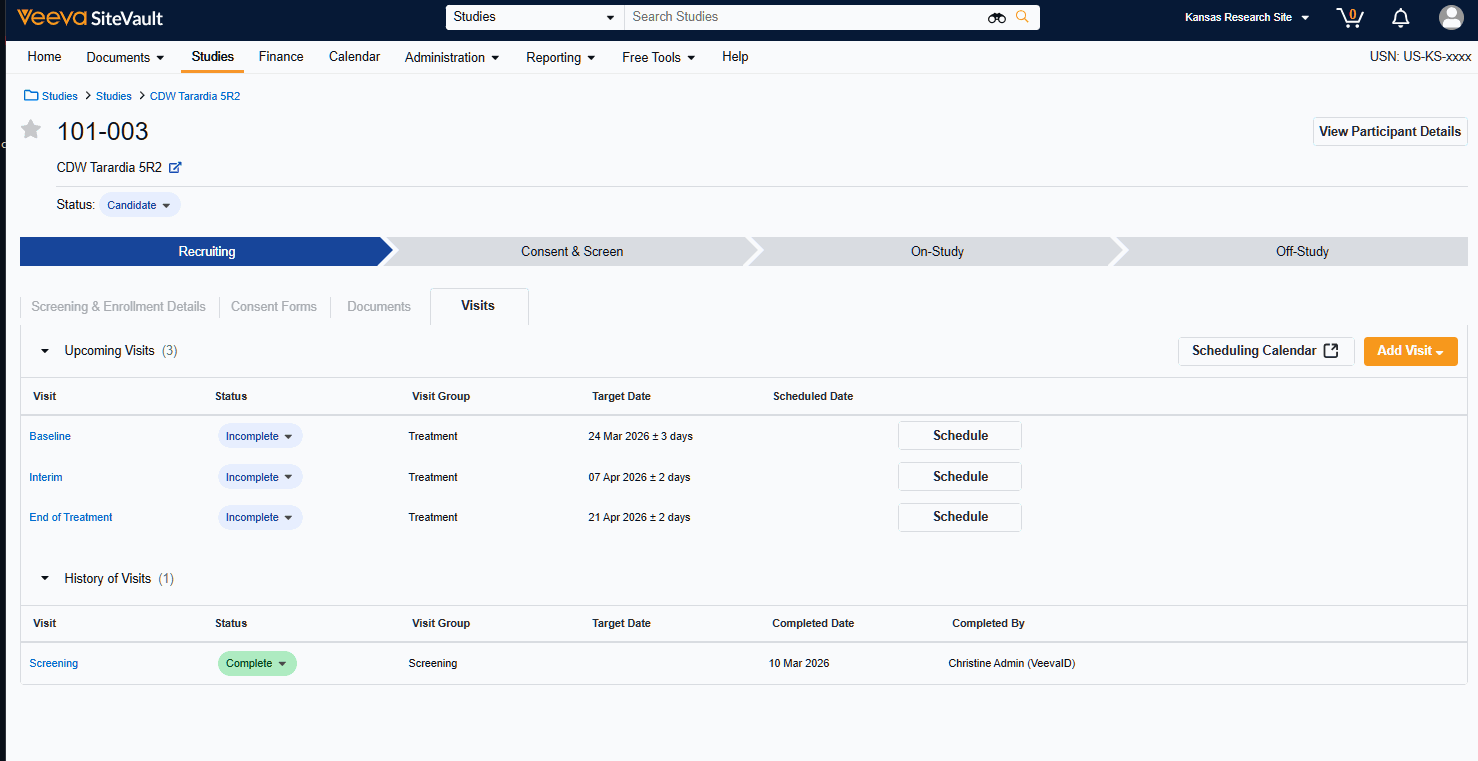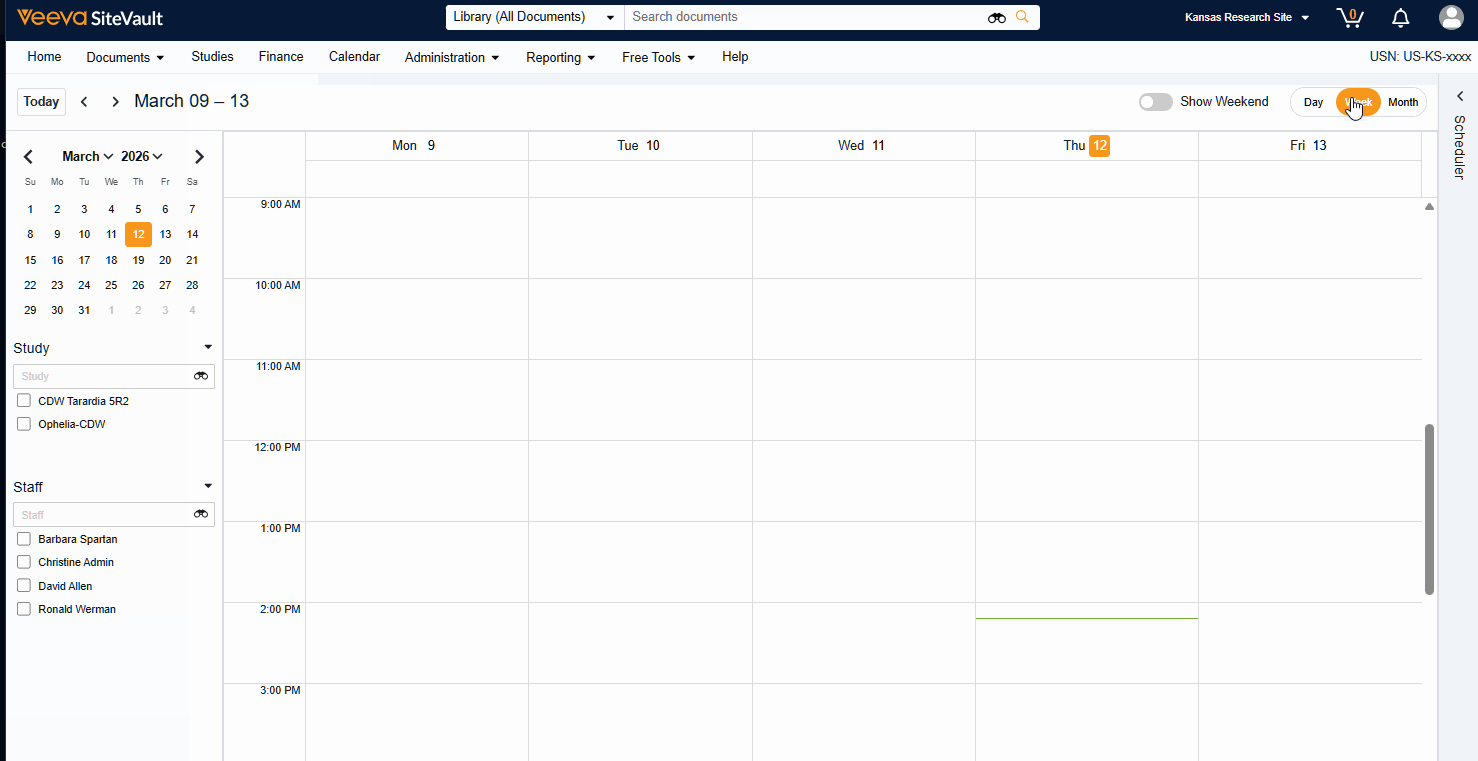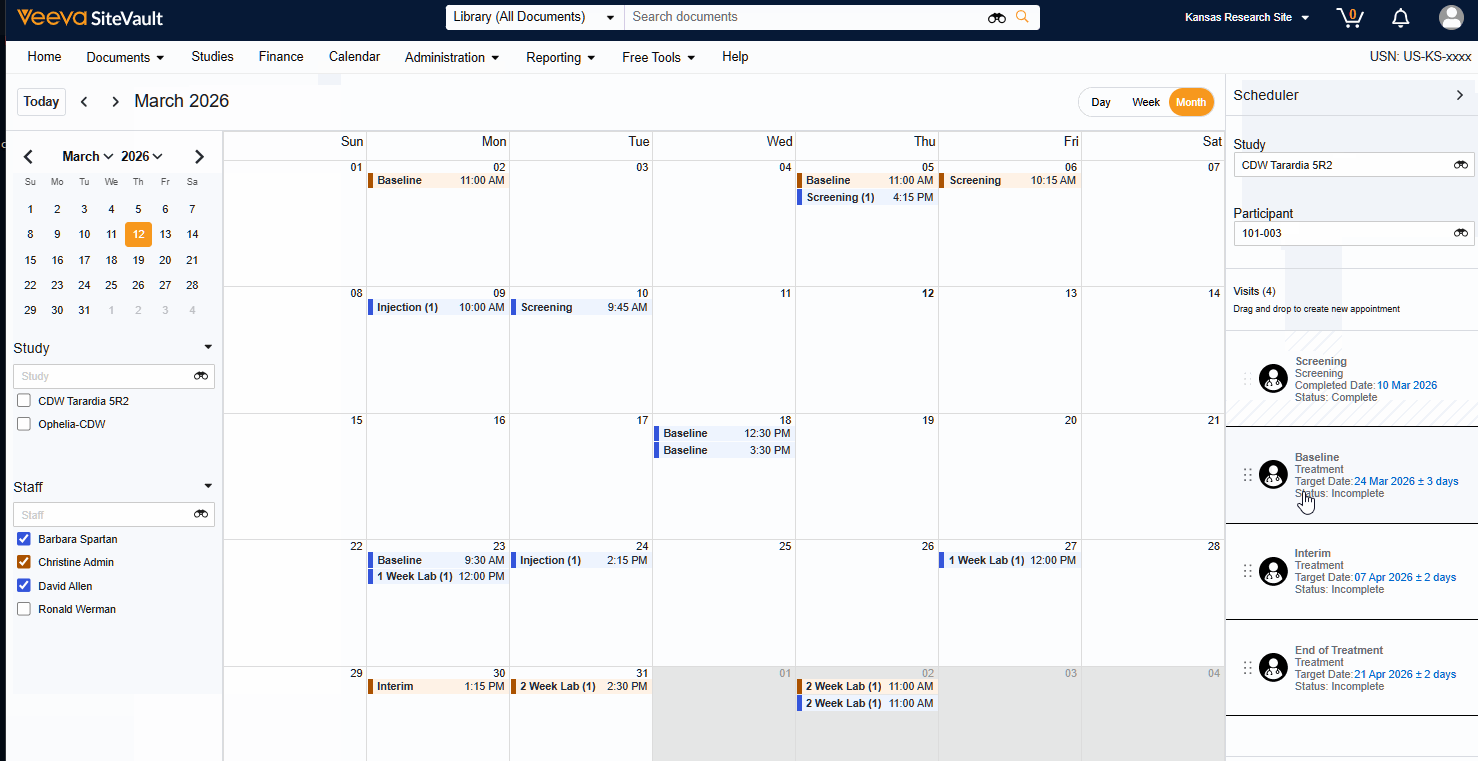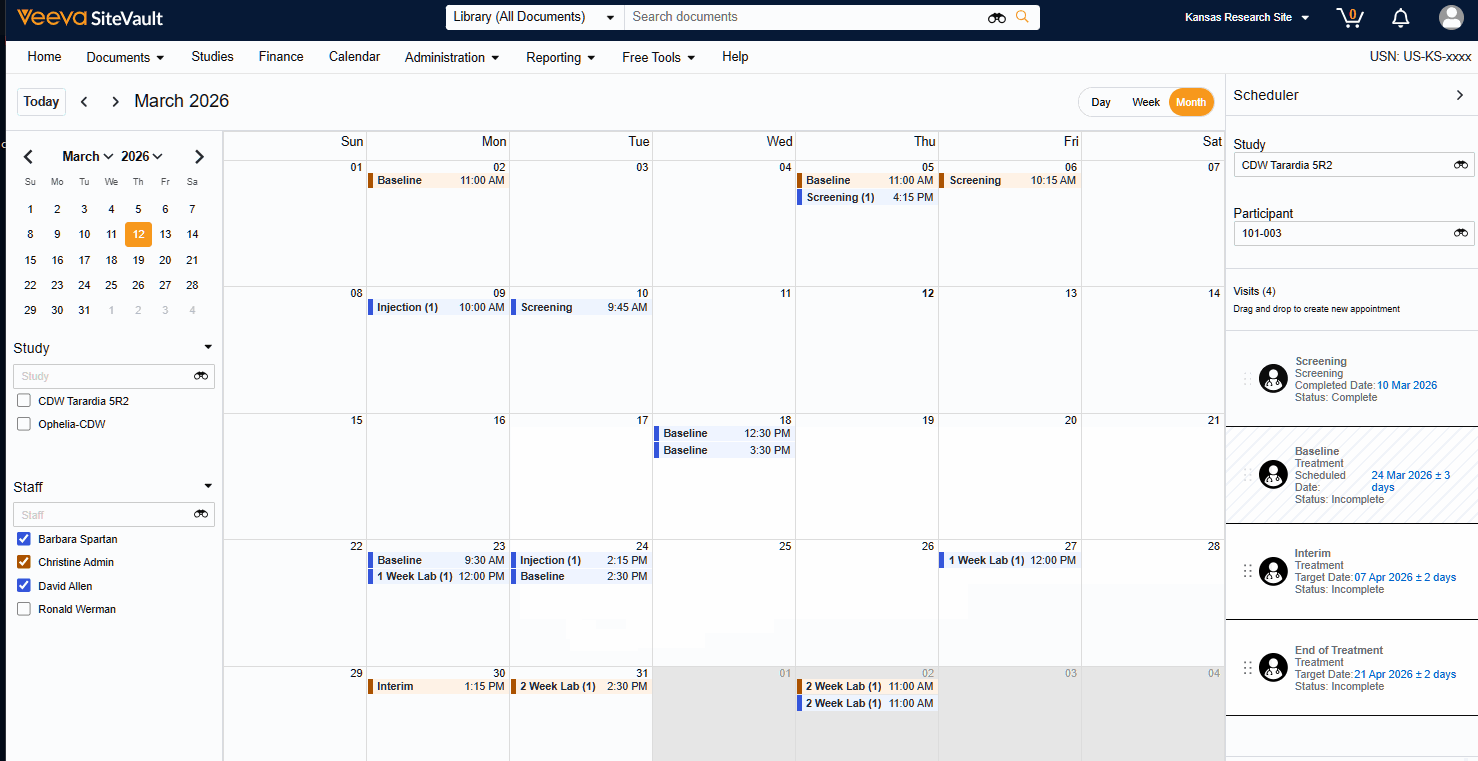
Der Besuchstermin bietet eine zentrale Übersicht über anstehende Termine der Studienteilnehmer und die zugehörigen Ressourcen. Diese Funktion wurde speziell für Prüfzentren entwickelt, die SiteVault CTMS als zentrales Datenerfassungssystem nutzen, und ermöglicht die Verwaltung von Studienplänen, Personalverfügbarkeit und Besuchstermine an einem Ort.
- Terminplanung für Besuchstermine: Erstellen und verwalten Sie Termine für bestimmte Besuchstermine zu festgelegten Daten und Uhrzeiten.
- Mitarbeiter Terminen zuordnen: Bestimmte Mitarbeiter werden den geplanten Besuchstermine zugeordnet, um die Arbeitsbelastung zu steuern.
- Zentrale Übersicht: Alle Termine aller Studien in einem einzigen, einheitlichen Kalender anzeigen.
- Erweiterte Filterung: Filtern Sie den zentralen Kalender nach Studie oder Mitarbeiter, um sich auf spezifische Terminplanungsbedürfnisse zu konzentrieren.
Veeva Study Training
Hier auswählen Eine vollständige Liste der Neuerungen in Veeva Study Training dieser Version finden Sie hier.
Anzeige von Schulungsaufgaben
Auf der Startseite für Lernende können Sie jetzt Trainingsaufgabenkarten (TA-Karten) für Kurse einsehen, für die Sie nicht angemeldet sind. Zuvor waren TA-Karten nicht sichtbar, wenn die Aufgabe nicht Teil eines Kurses war und die Selbstanmeldung nicht möglich war.
Direkte Verknüpfung mit Schulungsanforderungen für die Selbsteinschreibung
Mit diesem Update können Sie nun Selbstlernkurse über eine URL oder einen herunterladbaren QR-Code mit anderen Lernenden teilen. Wenn ein Empfänger auf den Link klickt oder den Code scannt, wird er automatisch zum Kurs auf seiner Startseite weitergeleitet und kann sich dort anmelden.
VeevaID
Hier auswählen Eine vollständige Liste der Neuerungen in dieser Version von VeevaID finden Sie hier.
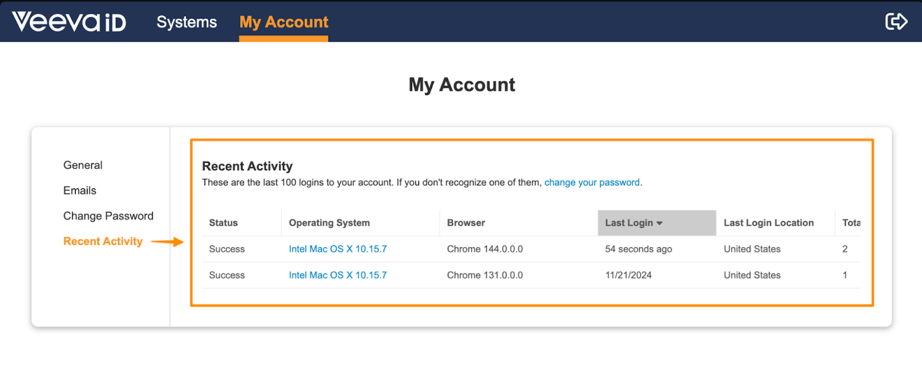
Aktuelle Aktivitäten bei VeevaID
VeevaID Nutzer haben ab sofort Zugriff auf den Bereich „Letzte Aktivitäten“ auf ihrer „Mein Konto“-Seite. Dort werden die letzten 100 Anmeldungen angezeigt. Diese Funktion ermöglicht es Nutzern, ihre Aktivitäten zu überwachen und so die Sicherheit ihres Kontos zu gewährleisten. Auf dieser Seite finden sich außerdem ein Link zum einfachen Ändern des Kennwort, falls verdächtige Anmeldungen festgestellt werden.
Es wurden keine Versionshinweise gefunden, die den ausgewählten Filtern entsprechen.