Formular 1572 erstellen und ausfüllen
Die Funktion „FDA-Formular 1572 generieren“ in Site Connect vereinfacht das Ausfüllen dieses wichtigen Dokuments. Anstatt für jede Studie wiederholt dieselben Informationen manuell einzugeben, nutzt Site Connect bereits im System gespeicherte Daten – wie z. B. Prüfzentrum und Mitarbeiterlisten –, um viele Teile des Formulars automatisch auszufüllen.
So füllen Sie das Formular aus
Wenn ein Sponsor oder ein CRO ein Formular 1572 anfordert, können Sie dieses auf der Registerkarte „Formulare“ generieren.
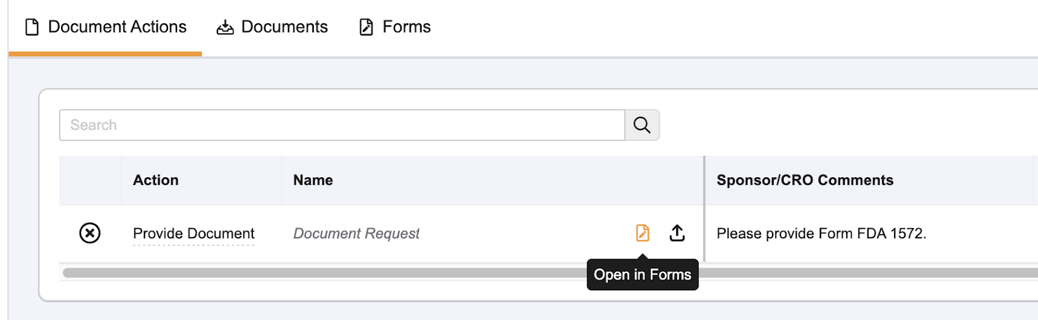
- Navigieren Sie zur Registerkarte „Dokumentenaustausch“.
- Suchen Sie die Aufgabe „Dokument bereitstellen“ für das Formular FDA 1572.
- Wählen Sie „In Formularen öffnen“ oder „Formulare“.
-
Überprüfen Sie die automatisch ausgefüllten Informationen im digitalen Formular. Site Connect ruft Daten ab für:
- Abschnitt 1: Name und Anschrift des Hauptforschers.
- Abschnitt 3, 4 und 5: Standorte der klinischen Studien, Labore und Informationen zur Ethikkommission.
- Abschnitt 6: Derzeit dem Projekt zugeordnete Unterforscher.
- Abschnitt 7 & 8: Protokolltitel, Nummer und Phase.
-
Falls Informationen fehlen oder aktualisiert werden müssen, klicken Sie auf das jeweilige Feld, um es zu bearbeiten.
- Hinweis: Bei der Entfernung von Mitarbeitern werden die Adressen auf „Inaktiv“ aktualisiert. Die Entfernung von Mitarbeitern löst automatisch eine Änderungsanforderung für das Prüfzentrum (SSCR) an den Sponsor aus, um die Richtigkeit Ihrer Prüfzentrum zu gewährleisten.
- Füllen Sie alle verbleibenden Pflichtfelder aus.
-
Wählen Sie nach Abschluss eine Einreichungsmethode aus:
- Zur elektronischen Signatur senden: Leitet das Formular zur elektronischen Unterschrift innerhalb von Site Connect an den Hauptforscher weiter.
- Download: Erzeugt ein ausfüllbares PDF für manuelle Unterschriften mit Tinte. Anschließend müssen Sie die unterschriebene Kopie wieder in die Aufgabe hochladen.
- Datei an SiteVault senden: (Falls eine Verbindung besteht) Sendet das Dokument direkt an Ihren SiteVault zur Ablage und Unterschrift.
Wissenswertes zur 1572-Funktion
- Anforderungen an die PI Unterschrift: Nur der Benutzer, dem in Site Connect die Rolle des Principal Investigator zugewiesen ist, kann das Formular elektronisch Unterschrift.
- Sofortige Aktualisierungen: Sie müssen nicht auf die Genehmigung eines SSCR durch einen Sponsor warten, um das Formular auszufüllen. Wenn Sie beim Ausfüllen des Formulars 1572 einen neuen Mitarbeiter oder eine neue Adresse hinzufügen, wird das Formular sofort aktualisiert, sodass Sie mit der Einreichung fortfahren können.
- Seite für elektronische Signaturen: Bei elektronischer Signatur in Site Connect wird am Ende der PDF-Datei ein Unterschrift (Bestätigungsseite) hinzugefügt. Die Unterschrift auf der ersten Seite des Formulars bleiben leer; dies ist das erwartete Verhalten für digitale Unterschriften.
- Abgelaufene Formulare: Site Connect aktualisiert die Vorlage 1572 automatisch, sobald die FDA eine neue Version veröffentlicht. So wird sichergestellt, dass Sie immer das aktuellste Formular verwenden.
- Prüfzentren außerhalb der USA: Auch wenn sich Ihr Prüfzentrum außerhalb der Vereinigten Staaten befindet, kann Ihr Sponsor dennoch verlangen, dass Sie dieses Formular ausfüllen, wenn die Studie im Rahmen eines Antrags auf Zulassung eines neuen Prüfpräparats (Investigational New Drug, IND) durchgeführt wird.