フォーム1572を作成して記入する
Site Connectの FDAフォーム1572生成 機能は、この必須文書の記入プロセスを簡素化するために設計されています。各試験ごとに繰り返し情報を手動で入力する代わりに、 Site Connectは、施設の施設やスタッフリストなど、システムに既に保存されているデータを使用して、フォームの多くの部分を自動的に入力します。
フォームの記入方法
試験依頼者またはCROから1572フォームの提出を求められた場合、 [フォーム] タブから生成できます。
- 「ドキュメントの授受」 タブに移動してください。
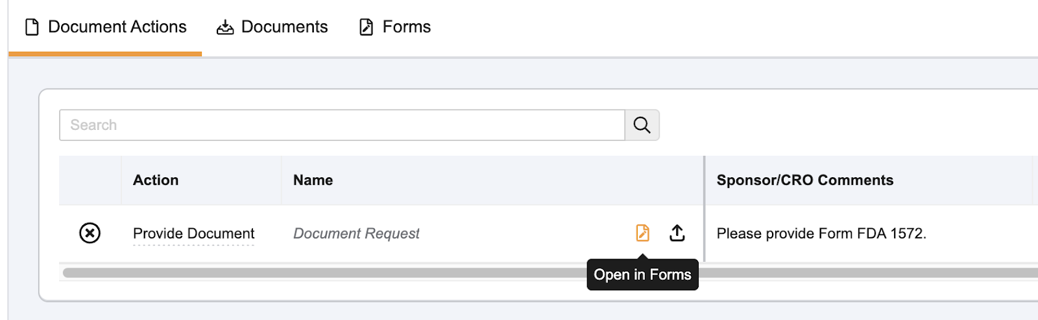
- FDAフォーム1572 の 「ドキュメント提出」 タスクを探してください。
- 「フォームで開く」 を選択するか、 「フォーム」 を選択してください。
-
デジタルフォームに自動入力された情報をレビュー。Site Site Connectは以下のデータを取得します。
- 第1項: 主任研究者の氏名および住所。
- セクション3、4、5: 臨床試験の実施場所、検査機関、および治験審査委員会(IRB)に関する情報。
- 第6項: 現在この試験に割り当てられている副研究者。
- セクション7および8: プロトコルのタイトル、番号、およびフェーズ。
-
情報が不足している場合や更新が必要な場合は、該当するフィールドをクリックして編集してください。
- 注: 削除された場合、住所は 「非アクティブ」 に更新されます。スタッフを削除すると、施設記録の正確性を維持するために、試験依頼者に対して 施設スタッフ変更依頼(SSCR) が自動的に送信されます。
- 残りの必須項目をすべて入力してください。
-
完了したら、送信方法を選択してください。
- 電子署名の送信: フォームを主任研究者に送信し、 Site Connect内で電子署名を行います。
- ダウンロード: 手書きの署名(インクによる署名)用の入力可能なPDFファイルを生成します。署名済みのコピーは、タスクにアップロードする必要があります。
- SiteVaultへのファイル送信:( 接続されている場合)ドキュメントをSiteVaultに直接送信して、ファイル保存と署名を行います。
1572機能について知っておくべきこと
- 主任研究 PIの署名要件: Site Connectで 主任研究者の 役割に割り当てられたユーザーのみが、フォームに電子署名を行うことができます。
- 即時更新: SSCRの承認を試験依頼者が待つ必要はありません。フォーム1572の入力中に新しいスタッフメンバーや住所を追加すると、フォームが即座に更新され、提出手続きを進めることができます。
- 電子署名ページ: Site Connectで電子署名を行うと、署名マニフェスト(確認ページ)がPDFの末尾に追加されます。フォームの最初のページにある署名欄は空白になりますが、これはデジタル署名における想定される動作です。
- 期限切れのフォーム: Site Connectは、 FDAが新バージョンをリリースすると1572テンプレートを自動的に更新し、常に最新のフォームを使用できるようにします。
- 米国以外の施設: たとえあなたの施設が米国外にある場合でも、試験が治験薬申請(IND)に基づいて実施される場合は、試験依頼者このフォームの記入を求められることがあります。