填写并完成表格 1572
Site Connect中的 FDA 1572 表格自动生成 功能旨在简化填写这份重要文件的流程。Site Site Connect无需您为每个研究手动输入重复信息,而是利用系统中已存储的数据(例如机构地址和员工名单)自动填写表格的许多部分。
如何填写表格
当申办方或 CRO 请求 1572 表格时,您可以在 “表单”选项 卡上生成该表格。
- 导航至 “文档交换”选项 卡。
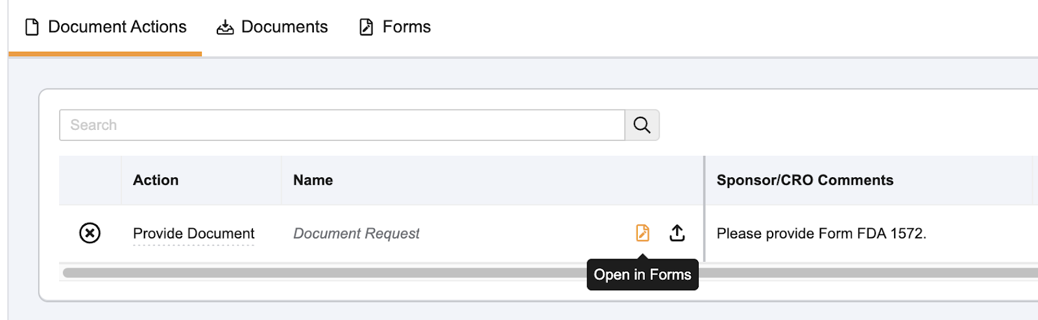
- 找到 FDA 1572 表格 的 “提供文件” 任务。
- 选择“ 在窗体中打开” 或选择 “窗体” 。
-
请查看电子表格中自动填充的信息。Site Site Connect会提取以下数据:
- 第一部分: 首席研究员姓名和地址。
- 第 3、4 和 5 部分: 临床试验地点、实验室和 IRB 信息。
- 第 6 部分: 目前分配到该研究的子研究员。
- 第 7 节和第 8 节: 协议标题、编号和阶段。
-
如果信息缺失或需要更新,请点击相应字段进行编辑。
- 注意: 如果移除,地址将更新为 “无效” 。移除员工将自动触发向申办方 提交的机构人员变更请求 (SSCR), 以确保您的机构记录保持准确。
- 请填写所有剩余的必填字段。
-
完成后,请选择提交方式:
- 发送电子签名: 将表单发送给首席研究员,以便在Site Connect中进行电子签名。
- 下载: 生成可填写的 PDF 文件,供手动“墨水签名”。签名后,您必须将签名副本上传回任务中。
- 文件上传至SiteVault:( 如果已连接)将文档直接发送到您的SiteVault进行归档和签名。
关于1572特征需要了解的事项
- PI签名要求: 只有在Site Connect中被分配为 首席研究员 角色的用户才能对表格进行电子签名。
- 即时更新: 您无需等待担保人批准 SSCR 即可完成表格。在填写 1572 表格时,如果您添加了新的员工或地址,表格会立即更新,您可以继续提交。
- 电子签名页: 在Site Connect中进行电子签名时,PDF 文件末尾会添加一个签名清单(确认页)。表单首页的签名栏将显示为空白;这是电子签名的正常现象。
- 过期表格: 当 FDA 发布新版本时, Site Connect会自动更新 1572 模板,确保您始终使用最新表格。
- 非美国机构: 即使您的机构位于美国境外,如果该研究是根据研究性新药 (IND) 申请进行的,您的赞助商仍可能要求您填写此表格。