양식 1572를 작성하고 제출하십시오.
Site Connect 의 FDA 양식 1572 생성 기능은 이 필수 문서를 작성하는 과정을 간소화하도록 설계되었습니다. 모든 연구에 대해 반복적인 정보를 수동으로 입력하는 대신, Site Connect 시스템에 이미 저장된 데이터(예: 사이트 기관 주소 및 직원 목록)를 활용하여 양식의 많은 부분을 자동으로 채워줍니다.
양식 작성 방법
스폰서 또는 CRO가 1572 양식을 요청하면 양식 탭에서 생성할 수 있습니다.
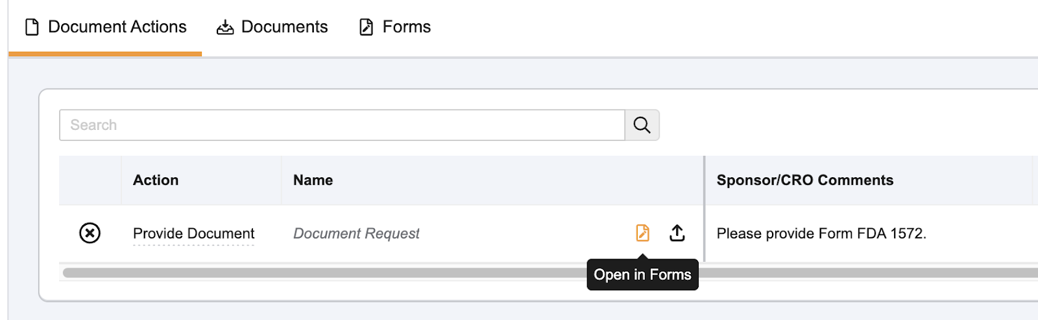
- 문서 교환 탭으로 이동하세요.
- FDA 양식 1572 에 대한 문서 제공 작업을 찾으십시오.
- '양식에서 열기'를 선택하거나 '양식'을 선택하세요.
-
디지털 양식에 자동으로 입력된 정보를 검토하세요. Site Connect 다음 항목에 대한 데이터를 가져옵니다.
- 제1절: 연구책임자 성명 및 주소.
- 제3, 4, 5절: 임상시험 장소, 실험실 및 IRB 정보.
- 제6절: 현재 연구에 배정된 하위 연구자.
- 제7절 및 제8절: 프로토콜 제목, 번호 및 단계.
-
정보가 누락되었거나 업데이트가 필요한 경우 해당 필드를 클릭하여 수정하세요.
- 참고: 직원이 삭제되면 주소는 '비활성' 으로 업데이트됩니다. 직원을 삭제하면 사이트 기록의 정확성을 유지하기 위해 후원 기관에 사이트 직원 변경 요청(SSCR)이 자동으로 전송됩니다.
- 나머지 필수 입력란을 모두 작성해 주세요.
-
완료되면 제출 방법을 선택하세요.
- 전자 서명 요청: 양식을 주 연구자에게 보내 Site Connect 내에서 전자 서명을 받도록 합니다.
- 다운로드: 수기로 서명할 수 있는 PDF 파일을 생성합니다. 서명된 PDF 파일을 다시 작업에 업로드해야 합니다.
- SiteVault 로 파일 전송: (연결된 경우) 문서를 SiteVault 로 직접 전송하여 보관 및 서명을 받을 수 있습니다.
1572년 특집 기사에 대해 알아야 할 사항
- PI 서명 요건: Site Connect 에서 연구책임자 역할로 지정된 사용자만 해당 양식에 전자 서명을 할 수 있습니다.
- 즉시 업데이트: 스폰서의 SSCR 승인을 기다리지 않고도 양식을 완료할 수 있습니다. 1572 양식을 작성하는 동안 새로운 직원이나 주소를 추가하면 양식이 즉시 업데이트되므로 제출을 진행할 수 있습니다.
- 전자 서명 페이지: Site Connect 에서 전자 서명을 하면 서명 확인 페이지(서명 명세서)가 PDF 파일의 끝에 추가됩니다. 양식의 첫 페이지에 있는 서명란은 비어 있게 되는데, 이는 디지털 서명의 정상적인 동작입니다.
- 만료된 양식: Site Connect FDA에서 새 버전을 출시하면 1572 템플릿을 자동으로 업데이트하여 항상 최신 양식을 사용할 수 있도록 합니다.
- 미국 이외 사이트: 임상시험 사이트 이 미국 이외 지역에 위치하더라도, 임상시험이 신약(IND) 신청에 따라 진행되는 경우 스폰서 측에서 이 양식을 작성하도록 요구할 수 있습니다.