I flussi di lavoro e le modifiche di stato vengono utilizzati per aggiornare lo stato dei documenti, certificare i documenti come copie o ottenere firme elettroniche sui documenti. Le task del flusso di lavoro assegnate all'utente vengono visualizzate nella vista "Le mie Task" nella scheda Home di SiteVault.
Esaminare il foglio di calcolo dei tipi di documento per determinare quali flussi di lavoro sono disponibili per ciascun tipo di documento SiteVault.
Panoramica dei flussi di lavoro dei documenti
Sotto la tabella puoi trovare maggiori informazioni su ciascun flusso di lavoro, nonché link alle singole pagine della guida sui flussi di lavoro e informazioni supplementari.
| Flusso di lavoro | Descrizione |
|---|---|
| Invia per l'approvazione della firma elettronica | Raccogli firme elettroniche sui documenti che richiedono una o più firme per l'approvazione. Non destinato alla supervisione PI. |
| Invia per firma elettronica | Disponibile per i tipi di documenti che richiedono una firma elettronica per un motivo specifico (solitamente indicato sul modulo). Ad esempio, CV, informativa finanziaria e modulo di consenso informato (firmato). |
| Invia per la firma elettronica dell'investigatore | Inviare il documento a uno o più ricercatori dello studio per la firma elettronica. Disponibile per i tipi di documento che richiedono la firma elettronica PI (in genere indicata sul modulo). Ad esempio, 1572 o equivalente, Accettazione dell'IB, Delega di Autorità e Pagina di Firma del Protocollo. |
| Invia per leggere e comprendere | Inviare uno o più documenti di studio ai membri del team di studio. Ogni destinatario deve confermare di aver letto e compreso ciascun documento di studio. |
| Invia per la revisione | Invia uno o più documenti ai colleghi che potranno fornire feedback utilizzando lo strumento di annotazione. |
Avvio dei flussi di lavoro
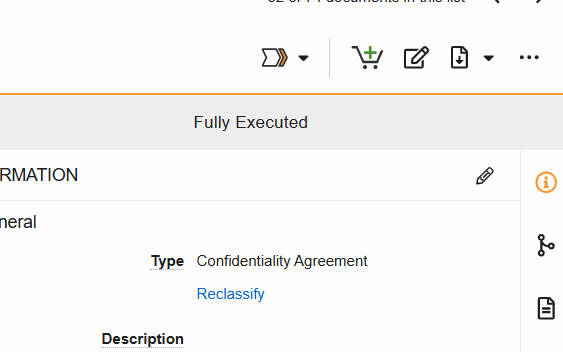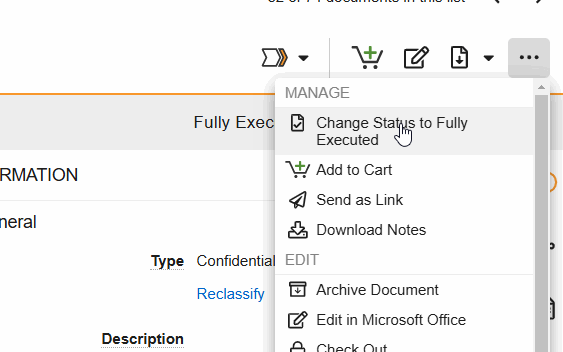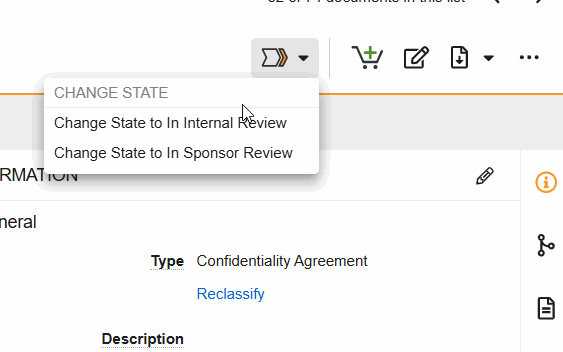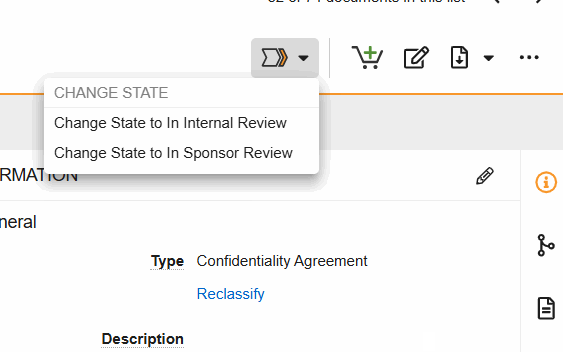
I flussi di lavoro vengono avviati dal menu Visualizzatore documenti > Azioni flusso di lavoro (vedere immagine) o dal menu Azioni documento (…) in Sede and Study eBinders.
Flussi di lavoro per firme elettroniche
Il flusso di lavoro eSignature di SiteVault consente Sedi di ricerca clinica di firmare elettronicamente documenti normativi e relativi allo studio, in conformità con i requisiti FDA 21 CFR Parte 11 e GCP. Ciò elimina la necessità di firme a inchiostro liquido e di gestione manuale dei documenti.
Principali vantaggi dell'adozione
- Conformità normativa: pienamente conforme alle normative sulla firma elettronica.
- Efficienza: riduce i tempi di elaborazione dei documenti firmati.
- Prontezza all'audit: fornisce una cronologia delle firme chiara e tracciabile.
- Accessibilità remota: consente di firmare da qualsiasi posizione, riducendo i ritardi.
Nota: la firma elettronica in SiteVault non è biometrica e richiede l'applicazione di due componenti distinti (un ID utente e una password) ed è conforme al requisito 21 CFR Parte 11 sezione §11.200 della Food and Drug Administration (FDA) per le firme elettroniche non basate sulla biometria.
Vuoi saperne di più?
Come utilizzare le firme elettroniche in SiteVault
Riepilogo delle funzionalità della firma elettronica
Avvio e completamento di flussi di lavoro multi-documento
Revisione del flusso di lavoro
Il flusso di lavoro di revisione consente al personale sede, ai monitor e ad altri soggetti interessati di rivedere e commentare i documenti all'interno SiteVault prima che vengano finalizzati. Ciò garantisce l'accuratezza e l'allineamento con i requisiti dello studio.
Principali vantaggi dell'adozione
- Collaborazione semplificata: consente feedback in tempo reale e riduce le revisioni dei documenti.
- Maggiore precisione: garantisce che i documenti soddisfino i requisiti normativi e di studio prima della finalizzazione.
- Ritardi ridotti: elimina lo scambio di e-mail e i processi di revisione manuale.
Vuoi saperne di più?
Come utilizzare il flusso di lavoro di revisione
Avvio e completamento di flussi di lavoro multi-documento
Leggi e comprendi il flusso di lavoro
Il flusso di lavoro "Leggi e comprendi" garantisce che il personale sede riconosca e comprenda i documenti critici, come le procedure operative standard (SOP) e i protocolli di studio. Tiene traccia del completamento e fornisce una documentazione di conformità pronta per la verifica.
Principali vantaggi dell'adozione
- Conformità migliorata: garantisce che il personale sia a conoscenza e comprenda i documenti essenziali.
- Prontezza all'audit: fornisce una chiara registrazione dei riconoscimenti.
- Efficienza: automatizza il monitoraggio e i promemoria per evitare ritardi.
Vuoi saperne di più?
Come utilizzare il flusso di lavoro Leggi e comprendi
Leggi e comprendi il riepilogo delle funzionalità
Avvio e completamento di flussi di lavoro multi-documento
Modifiche allo stato del documento SiteVault
- Cambia stato in (stato finale): porta il documento al suo stato stabile. Questo cambio di stato include l'opzione per eseguire la certificazione della copia.
- Cambia stato in revisione interna: indica che il documento è in fase di revisione interna.
- Cambia stato in In revisione sponsor: indica che il documento è in fase di revisione dello sponsor.