Veeva eConsentは、試験参加者、署名者、そして治験施設のスタッフがインフォームド・同意書(ICFs)に電子的に署名することを可能にします。これにより、フォームの印刷が不要になり、同意取得プロセスが迅速化されます。参加者とその署名者は、オフィスや自宅で使い慣れたデバイスでフォームをレビュー、自分のペースで読むことができます。また、フォームを簡単にダウンロードして家族やケアチームと共有することもできます。さらに、アクセシビリティが必要な参加者は、拡大表示やスクリーンリーダーの利用も可能です。
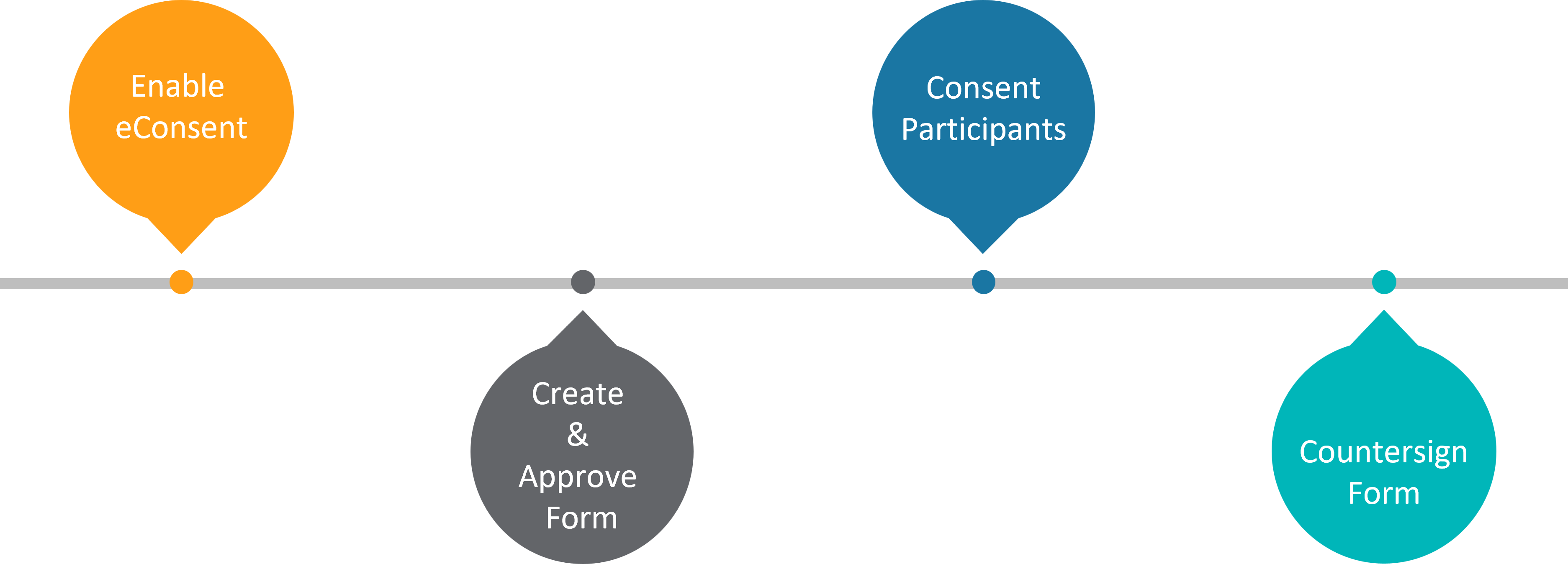
eConsentフォームの作成と管理
SiteVault は、次のために必要なすべてのツールを提供します。
- eConsent書を作成する
- eConsent書の編集
- レビューのためにeConsent書を共有する
- eConsent書の使用を承認する
患者の同意オプション
Veeva eConsent は、患者の安心レベルを満たすことができる複数の同意オプションを施設に提供します。
- リモートeConsent: 患者は、 MyVeeva for Patientsアプリケーションを使用してモバイル デバイスから電子的に署名できます。
- オンサイトeConsent: 患者は貴社のテクノロジーを使用して貴社の施設で電子的に署名できます。
- オンサイトウェット署名: 患者に署名してもらう同意書を印刷できます。
リモート エクスペリエンスを表示するには、 リモートeConsentインタラクティブ デモ を参照してください。
eConsentの追跡と管理
署名が完了すると、 eConsentへの回答内容は同意書のオンラインレンダリングで確認でき、システムに保存されるため、効率的なレビューと検索が可能です。なお、署名済みICFに記録されるすべての署名のタイムゾーンは試験施設の所在地に基づいており、アクティブユーザーのタイムゾーンやSiteVaultでユーザーに表示されるタイムゾーンと一致しない場合がありますので、ご注意ください。
eConsentドキュメントフォーマット(eConsentタイプ)
eConsentフォームは、PDFファイルまたはDOCX(Word)形式でアップロードできます。SiteVaultにドキュメントをインポートしてeConsentフォームを作成すると、ファイル形式はフォームの有効期間中(後続のバージョンを含む)維持されます。アップロード後は、 SiteVaultのeConsentエディターを使用して質問と署名要素を追加できます。
eConsentエディター
PDFベースのeConsentエディター
PDFベースのeConsentエディターを使用すると、施設ユーザーは質問や署名要素をPDF同意書に直接重ねることができます。IRB承認済みのPDF同意書をアップロードすることで、デジタル化後のIRBによる追加審査を回避できます。
カスタムeConsentビルダー (Microsoft Word™)
Word ベースのドキュメントからコンテンツをインポートし、カスタムeConsentビルダーで編集して署名ブロック、質問ブロック、画像、ビデオなどの項目をフォーマットすることで、 eConsentフォームを作成できます。
ブラウザとデバイスの前提条件
eConsentエディターを最適に使用するには、ブラウザーとデバイスが次の要件を満たしていることを確認してください。
- ブラウザ: エディターにはデスクトップブラウザのご利用を推奨します。Google Chrome、Microsoft Edge、またはMozilla Firefoxをご利用いただくと、最適なエクスペリエンスをお楽しみいただけます。
- ポップアップ ブロッカー: Apple Safari または Mozilla Firefox を使用してeConsentフォームを編集する場合は、 SiteVault Web サイトからのポップアップを許可するようにブラウザを設定する必要があります。
- 解決策: 画面の幅が 960 ピクセルより小さい場合、または同等の幅に拡大表示した場合、目次やSiteVaultへの保存やチェックインのボタンなどの一部の機能を使用できないことがあります。